中山大學(xué)附屬第八醫(yī)院(深圳福田)臨床試驗倫理委員會簡介及聯(lián)系方式
?一、臨床試驗倫理委員會主要職責(zé):
1.?起草、修訂和審議本倫理委員會的制度、標(biāo)準(zhǔn)操作規(guī)程、審查指南等審查具體執(zhí)行條款,提請機構(gòu)倫理委員會審議。
2.?負(fù)責(zé)對醫(yī)院院本部及社康中心范圍內(nèi)開展的藥物、器械、診斷試劑等臨床試驗項目的倫理審查。
3.?為臨床試驗申請項目提供倫理審查咨詢。
4.?按規(guī)定接受上級衛(wèi)生行政管理部門和/或食品藥品監(jiān)督管理部門督導(dǎo)檢查,并向機構(gòu)倫理委員會報告年度倫理審查工作情況。
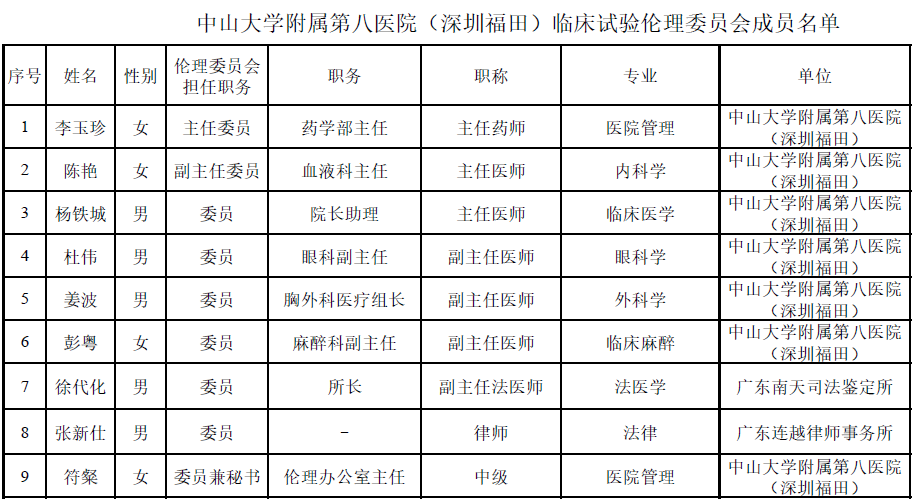
?二、成員組成:臨床試驗倫理委員會最近一次調(diào)整為2022年8月,設(shè)主任委員1名,副主任委員1名,委員7名,總數(shù)為9名,其中男性5名,女性4名。
?三、臨床試驗倫理委員會審查收費標(biāo)準(zhǔn)
1.初始審查收費標(biāo)準(zhǔn):
1.1?符合會議審查要求,評審費6000元/項。
1.2?符合簡易審查要求,評審費3000元/項。
1.3?申辦方因項目進(jìn)度需加急進(jìn)行審查,在征求倫理委員會主任委員同意后,可考慮申請加急,并另繳納緊急費1500元/項。(具體請詢倫理辦公室)
2.復(fù)審收費標(biāo)準(zhǔn):
作必要的修正后同意項目及申辦方有異議提出復(fù)審,可由倫理委員會主任委員決定采用會議審查或簡易審查,評審費均為3000?元/項。
3.跟蹤審查收費標(biāo)準(zhǔn):
3.1?非預(yù)期嚴(yán)重不良反應(yīng)事件(SUSAR)審查、年度/定期跟蹤審查、暫停/終止研究審查、結(jié)題審查不收取費用。
3.2?修正案審查,評審費3000元/項。
3.3?違背方案審查,評審費2000元/季度。
※以上收費標(biāo)準(zhǔn)均已含稅。
四、聯(lián)系方式:
臨床試驗倫理委員會聯(lián)系地址:深圳市福田區(qū)福華路92號中大八院行政樓406倫理辦公室
聯(lián)系電話:0755-82563178(正常工作日8:00-12:00,14:00-17:00)
電子郵箱:[email protected](持續(xù)更新)
※申辦方相關(guān)人員聯(lián)系倫理審查業(yè)務(wù)時請使用公司后綴的個人郵箱,并在郵件主題開頭注明“GCP+公司及項目簡稱”字樣,郵件中至少應(yīng)說明①申辦方名稱、②該聯(lián)系郵箱人員姓名及身份、③項目名稱、④項目承辦科室及PI姓名。倫理辦公室將及時發(fā)送相關(guān)詳細(xì)指引。
聯(lián)系人:符粲
?





